- Investigadores del Centro de Investigación del Cáncer (CIC-IBMCC) y del CIBER de Cáncer (CIBERONC), dirigidos por Xosé Bustelo, identifican un nuevo programa patológico asociado a la inducción y mantenimiento de propiedades malignas de los cánceres de cabeza y cuello que van asociados a bajas tasas de supervivencia de los pacientes.
- Este programa está frecuentemente alterado en pacientes con cánceres de cabeza y cuello malignos.
- Los investigadores han demostrado que esta desregulación confiere propiedades malignas a las células sanas y, en combinación con otras alteraciones genéticas, al desarrollo más rápido de tumores.
- También han demostrado que la inactivación de elementos clave de este programa patológico conlleva la reversión de las células tumorales a un comportamiento similar a las sanas.
- Este trabajo ha identificado dianas terapéuticas con potencial interés para el desarrollo futuro de fármacos para combatir este tumor. También describe una firma diagnóstica que permite identificar a pacientes con mal pronóstico en función del perfil genético presente en sus tumores.
Los cánceres de cabeza y cuello se originan a partir de alteraciones genéticas en las células que recubren la mucosa bucal y del tracto respiratorio superior como la lengua, laringe y faringe. Factores de riesgo que determinan la aparición de estos cánceres incluyen la ingesta de alcohol, humo del tabaco e infecciones por el virus del papiloma humano. Estos tumores son actualmente un reto clínico, dada sus altas cotas de incidencia a nivel mundial, sus bajos porcentajes de supervivencia de pacientes y la falta de fármacos adecuados.
Una de las características que determinan la malignidad de estos tumores es la detección en las biopsias de células cancerosas altamente proliferativas y que están en un estado muy indiferenciado. Debido a ello, se considera que fármacos que puedan revertir estas propiedades biológicas podrían tener un impacto importante en el tratamiento de este subtipo de pacientes. Lamentablemente, el desarrollo de este tipo de fármacos está lastrado por el desconocimiento que todavía existe sobre las rutas biológicas específicas que determinan la aparición y el mantenimiento de las características malignas de estos tumores.
En este trabajo, los investigadores del Centro de Investigación del Cáncer y del CIBER de Cáncer han descubierto una ruta de señalización activada por la molécula VAV2 que es esencial para el desarrollo y evolución de estas características malignas. El hallazgo se ha publicado en la revista Nature Communications.
“La pista inicial para este trabajo la dieron estudios bioinformáticos de datos genómicos de tumores, los cuales que revelaron que la expresión de esta molécula está muy elevada en una proporción muy elevada de pacientes con cánceres de cabeza y cuello”, indica Xosé Bustelo, el director de este trabajo. “Estos estudios también revelaron que los niveles de expresión de esta molécula estaban asociados con un mal pronóstico para estos pacientes. Esto nos llevó a estudiarla en más detalle”.
Para establecer el papel de esta molécula, el grupo generó en primer lugar un ratón modificado genéticamente que reproducía el patrón de desregulación de VAV2 en presente en los tumores humanos. “Esto permitió descubrir que la activación descontrolada de VAV2 alteraba el comportamiento de las células normales, llevándolas a reproducir las características más iniciales de estos tumores. Además, en combinación con otras alteraciones genéticas, vimos que estos ratones podían desarrollar tumores muy rápidamente”, añade Bustelo. “El análisis posterior de estas células permitió descubrir que habían adquirido unas características altamente proliferativas e indiferenciadas, lo que en la jerga científica se conoce por un estado de proliferación regenerativa”, añade Francisco Lorenzo-Martin, uno de los autores principales de este trabajo. Además, este estudio permitió desentrañar el programa patológico activado por VAV2 implicado en este proceso patológico, lo que permitió identificar nuevas dianas terapéuticas y firmas diagnósticas.
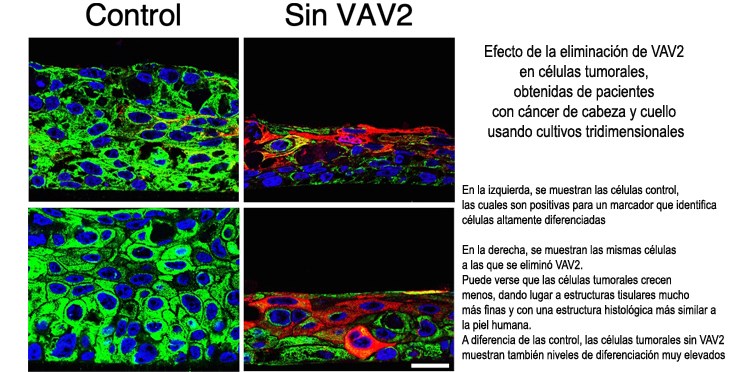
Los investigadores también pudieron demostrar que la expresión de VAV2 era crucial para mantener estos rasgos malignos en las células cancerosas directamente obtenidas de pacientes. Debido a ello, la eliminación de VAV2 y de otros elementos clave de su ruta biológica hace que las células cancerosas reviertan a un estado similar al mostrado por las células sanas. “Este último punto reafirma la importancia que esta ruta tiene en los tumores de pacientes”, indica Natalia Fernández-Parejo, una de las investigadoras que ha trabajado también en este proyecto. “También indica que la inhibición farmacológica de VAV2 y de varios elementos que participan en este proceso patológico pueden tener interés terapéutico”, indica Lorenzo-Martín. Enfatizando esta posible aplicación, este grupo de investigación había demostrado hace unos meses que la inhibición de la actividad de VAV2 no induce ningún daño colateral en los órganos sanos.
Aunque este trabajo representa un avance a nivel básico, los resultados más directamente trasladables a la clínica son unas firmas genéticas que se podrán utilizar para pronosticar la evolución de pacientes con cáncer de cabeza y cuello. También ha revelado los puntos clave de esta ruta que podrían ser usados para el desarrollo de fármacos específicos contra esta enfermedad. De hecho, el trabajo demostró a nivel preclínico que algunos compuestos químicos que inhiben la actividad de algunos de estos elementos de este programa patológico VAV2-dependiente también podían revertir estas características malignas de las células tumorales.
El grupo del Dr. Bustelo está compuesto por miembros pertenecientes al CSIC, la Universidad de Salamanca, la Fundación para la Investigación del Cáncer de Salamanca y el CIBER de Cáncer. Contó también con la colaboración de otros científicos pertenecientes al CIBER de Cáncer (CIBERONC) y de Enfermedades Respiratorias (CIBERES), al Centro de Investigaciones Medioambientales (CIEMAT) de Madrid, al Centro de Investigación de Medicina Molecular y Enfermedades Crónicas de Santiago de Compostela, al IRB de Barcelona, al Hospital Universitario de Oviedo, al Instituto de Investigación Biosanitaria de Salamanca y a dos centros de investigación argentinos.
La financiación de este trabajo ha sido posible gracias a proyectos concedidos por la Worldwide Cancer Research del Reino Unido, el Ministerio de Ciencia e Innovación, el Ministerio de Universidades, el Instituto de Salud Carlos III, la Asociación Española contra el Cáncer (AECC) y la Junta de Castilla-León. Recientemente el grupo de investigación ha recibido también financiación por parte de la Fundación La Caixa para un proyecto de investigación independiente centrado en linfomas.
Referencia del artículo
VAV2 signaling promotes regenerative proliferation in both cutaneous and head and neck squamous cell carcinoma
L. Francisco Lorenzo-Martín, Natalia Fernández-Parejo, Mauricio Menacho-Márquez, Sonia Rodríguez-Fdez, Javier Robles-Valero, Sonia Zumalave, Salvatore Fabbiano, Gloria Pascual, Juana García-Pedrero, Antonio Abad, Carmen García-Macías, Nazareno González, Pablo Lorenzano-Menna, Miguel A. Pavón, Rogelio González-Sarmiento, Carmen Segrelles, Jesús M. Paramio, José M.C. Tubío, Juan P. Rodrigo, Salvador A. Benitah, Myriam Cuadrado & Xosé R. Bustelo (2020).
Nature Communications, 22 de septiembre 2020
Sobre el CIC
El Centro de Investigación del Cáncer es un centro mixto del CSIC y la Universidad de Salamanca que se caracteriza por el desarrollo de líneas de investigación multidisciplinares que permitan avances en el conocimiento del cáncer y su traslación al ámbito clínico. Ofrece también plataformas tecnológicas y diagnóstica de utilidad para centros académicos e industrias pertenecientes tanto a Castilla y León como del resto de España. Muchos de sus integrantes están integrados en el CIBERONC y dirigen Unidades de Investigación Cooperativa reconocidas por la Junta de Castilla y León. Recientemente, ha sido reconocido como Centro de Excelencia por la Junta de Castilla y León.
Sobre CIBERONC
El Centro de Investigación Biomédica en Red (CIBER) es un consorcio dependiente del Instituto de Salud Carlos III (Ministerio de Economía, Industria y Competitividad) y cofinanciado con fondos FEDER. Su área temática de Cáncer (CIBERONC) está formada por 50 grupos de investigación pertenecientes a 27 instituciones consorciadas entre hospitales, universidades y centros de investigación. Estos grupos multidisciplinares trabajan conjuntamente en seis grandes Programas de Investigación: Cáncer de colon y tracto digestivo, Cáncer de mama, Cáncer de pulmón y vías respiratorias, Tumores hematológicos, Tumores de baja prevalencia y Mecanismos moleculares de la progresión tumoral. Éste último es al que pertenece el grupo del Dr. Xosé R. Bustelo. Esta área CIBERONC fue creada de forma específica para ofrecer una plataforma colaborativa óptima con la que integrar la excelente investigación básica que se realiza actualmente en España en la realidad clínica.


