El desarrollo de la cantidad adecuada de músculo viene determinado por unos mensajeros de nuestro cuerpo muy especializados, denominados científicamente como hormonas, que pertenecen a la familia de la insulina. Estas hormonas cuando llegan al músculo dan órdenes para que se favorezca tanto la formación de nuevo músculo como el aumento de la masa muscular a lo largo del tiempo. Debido a ello, cambios en estos mensajeros o sus vías de señalización pueden determinar el crecimiento anormal del músculo, su reducción o atrofia. A pesar de ello, todavía desconocemos mucho sobre los procesos biológicos que están detrás de la generación de un “Popeye” musculoso o una “Olivia” con muy poco músculo.
En el trabajo que se acaba de publicar en la revista Nature Communications, investigadores del Centro de Investigación del Cáncer y los CIBER de Cáncer y de Obesidad y Nutrición, liderados por Xosé Bustelo, han descubierto una nueva ruta de señalización regulada por la molécula VAV2 que juega papeles críticos en la regulación de la masa muscular.
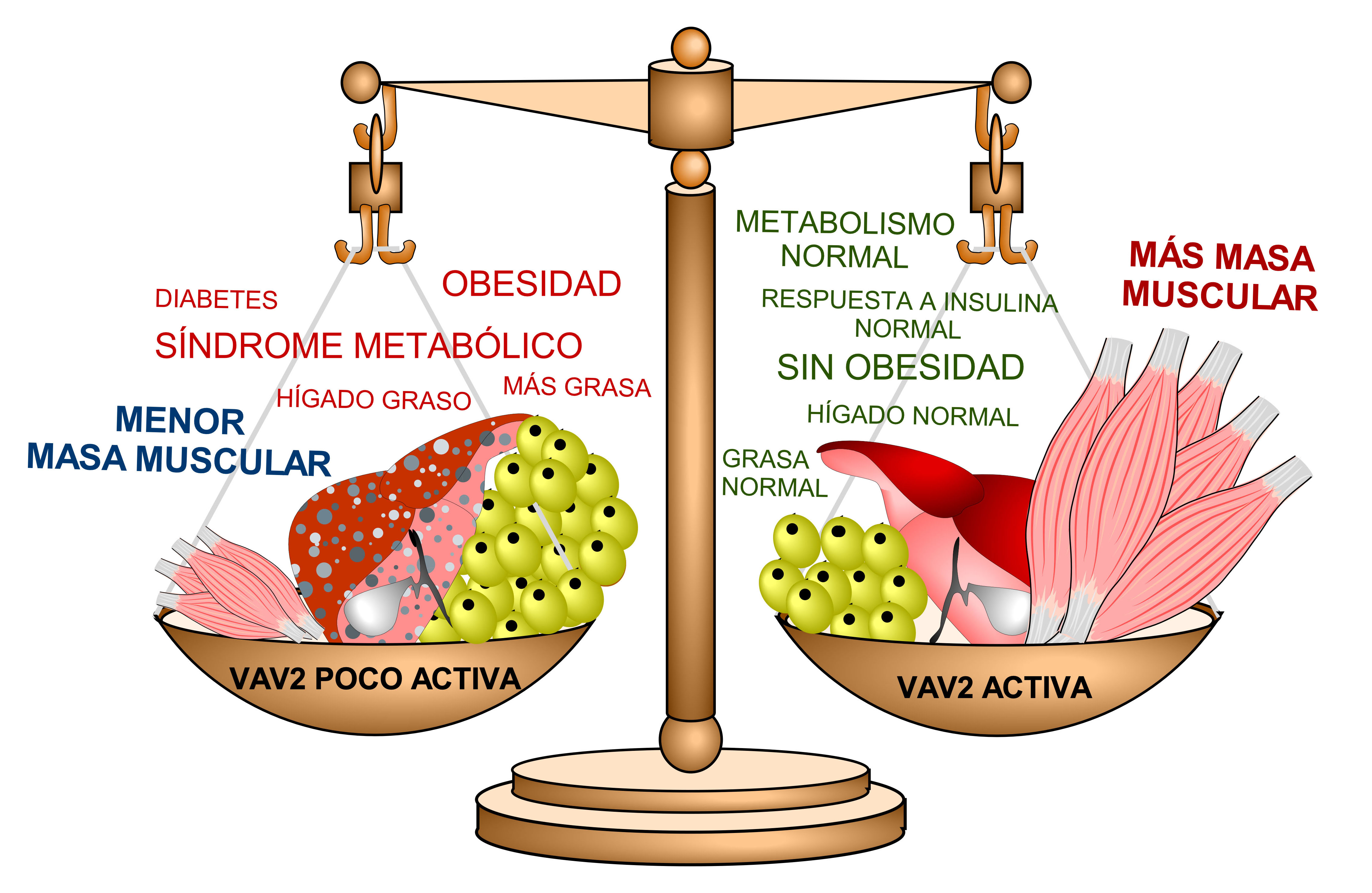
Para realizar este hallazgo, el grupo de investigación generó dos tipos de ratones modificados genéticamente que alteraban la actividad biológica de VAV2. “Con el primer modelo experimental, que expresaba una forma activada de VAV2, vimos que el ratón desarrollaba una gran cantidad de masa muscular. En cambio, el segundo tipo de ratón, el cual expresaba una forma poco activa de VAV2, presentaba una masa muscular muy reducida. Esto nos indicó de forma clara que esta molécula tenía que ejercer un papel crucial en la determinación de la masa molecular de nuestro organismo”, señala Xosé Bustelo, el líder científico de los grupos de investigación que llevaron a cabo este trabajo. “Los estudios posteriores nos revelaron que la función de VAV2 era la de favorecer la acción de la insulina y hormonas relacionadas en el interior de las células del músculo. Esto, a su vez, nos llevó tras varios años de trabajo a descubrir el mecanismo específico por el cual ejercía dicha función”, añade Sonia Rodríguez Fernández, la científica que firma como primera autora en este trabajo. “VAV2 parece funcionar, por tanto, como las espinacas de Popeye: cuando está muy activado contribuye a desarrollar mucho músculo y, cuando está poco activo, hace que disminuya la masa muscular”, añade Rodríguez Fernández.
Los investigadores también pudieron ver que los ratones que poseían mayor masa muscular mostraban unas características más sanas y, cuando se les añadía una dieta rica en grasa, no desarrollaban obesidad. Por el contrario, los ratones que poseían menos músculo debido a una baja actividad de VAV2 se convertían en obesos de forma espontánea y, cuando se les añadía una dieta rica en grasa, engordaban mucho más que los animales control. Y, asociado a ello, desarrollaban problemas típicamente vinculados con la obesidad como, por ejemplo, la diabetes. “Estos datos nos recuerdan el papel fundamental que tiene el músculo para mantener un equilibrio metabólico adecuado a largo plazo en nuestro organismo”, indica Xosé Bustelo. “También indican que estar delgado es obviamente beneficioso para mantener nuestra salud, pero eso no es así si la pérdida de peso se hace a expensas de perder masa muscular”, indica Sonia Rodríguez Fernández.
El grupo del Dr. Bustelo está compuesto por miembros pertenecientes al CSIC, la Universidad de Salamanca, la Fundación para la Investigación del Cáncer de Salamanca y el CIBER de Cáncer. Contó también con la colaboración de otros científicos pertenecientes al CIBER de Fisiopatología de la Obesidad y Nutrición (CIBEROBN) y de las universidades de Santiago de Compostela y Ginebra (Suiza).
La financiación de este trabajo ha sido posible gracias a proyectos concedidos por el Ministerio de Ciencia e Innovación, el Ministerio de Universidades, el Instituto de Salud Carlos III, la Asociación Española contra el Cáncer (AECC) y la Junta de Castilla-León.
Sobre el CIC
El Centro de Investigación del Cáncer (CIC-IBMCC) es un centro mixto del CSIC y la Universidad de Salamanca que se caracteriza por el desarrollo de líneas de investigación multidisciplinares que permitan avances en el conocimiento del cáncer y su traslación al ámbito clínico. Ofrece también plataformas tecnológicas y diagnóstica de utilidad para centros académicos e industrias pertenecientes tanto a Castilla y León como del resto de España. Muchos de sus integrantes están integrados en el CIBERONC y dirigen Unidades de Investigación Cooperativa reconocidas por la Junta de Castilla y León. Recientemente, ha sido reconocido como Centro de Excelencia por la Junta de Castilla y León.
Sobre CIBERONC
El Centro de Investigación Biomédica en Red (CIBER) es un consorcio dependiente del Instituto de Salud Carlos III (Ministerio de Economía, Industria y Competitividad) y cofinanciado con fondos FEDER. Su área temática de Cáncer (CIBERONC) está formada por 48 grupos de investigación pertenecientes a 27 instituciones consorciadas entre hospitales, universidades y centros de investigación. Estos grupos multidisciplinares trabajan conjuntamente en seis grandes Programas de Investigación: Cáncer de colon y tracto digestivo, Cáncer de mama, Cáncer de pulmón y vías respiratorias, Tumores hematológicos, Tumores de baja prevalencia y Mecanismos moleculares de la progresión tumoral. Éste último es al que pertenece el grupo del Dr. Xosé R. Bustelo. Esta área CIBERONC fue creada de forma específica para ofrecer una plataforma colaborativa óptima con la que integrar la excelente investigación básica que se realiza actualmente en España en la realidad clínica.
Referencia del artículo:
Vav2 catalysis-dependent pathways contribute to skeletal muscle growth and metabolic homeostasis
Sonia Rodríguez-Fdez, L. Francisco Lorenzo-Martín, Isabel Fernández-Pisonero, Begoña Porteiro, Christelle Veyrat-Durebex, Daniel Beiroa, Omar Al-Massadi, Antonio Abad, Carlos Diéguez, Roberto Coppari, Rubén Nogueiras, and Xosé R. Bustelo (2020).
Nature Communications, 16 de octubre de 2020
Enlace: doi 10.1038/s41467-020-19489-z